Eloxieranleitung - 2. Grundlagen
|


|
2.1 Die Eigenschaften der Schicht
Blankes Aluminium oxidiert an der Luft sehr schnell, überzieht sich dabei allerdings mit einer luftundurchlässigen
farblosen Oxidschicht (Al2O3). Diese sehr dünne (typischerweise 0,5-1µm dicke) Schicht schützt das Metall vor
weiterem Angriff des Luftsauerstoffs. Sie ist recht weich und unansehnlich und genügt wegen ihrer sehr geringen
Stärke keinen höheren Ansprüchen. Allerdings kann man durch gezielten Aufbau dieser Schicht mit Hilfe eines
wässrigen Elektrolyten folgende Eigenschaften herausbilden:
- Härte: etwa Mohs-Härte 9 (Korund); Quarz hat Härte 7, Diamant Härte 10
- Schichtdicke: abhängig von Spannung, Baddauer und weiteren Parametern 5-250 µm (0,005-0,25 mm)
- Durchschlagsfestigkeit: ca. 30 Volt pro µm
- Farbe: farblos bis gräulich/schwärzlich (je nach Legierung); bei geeigneten Legierungen bleibt das metallische Aussehen des
darunterliegenden Aluminiums erhalten - auch bei späterer Einfärbung.
- mit geeigneten Farbstoffen kratzfest und lichtecht einfärbbar; mögliche Kombinationen mehrerer Farbstoffe
ermöglichen fast jeden beliebigen Farbton
2.2 Chemische Reaktion
Im Eloxierbad laufen im Wesentlichen folgende chemischen Reaktionen ab:

Es fallen zwei Dinge ins Auge:
- Die Bildung der Schicht an sich benötigt keine Schwefelsäure. Sie dient als Elektrolyt (dies
verringert massiv den elektrischen Widerstand des Bades) und - das ist der wichtigere Part - löst die Schicht lokal auf und sorgt so
für weiteren Stromfluss und Schichtaufbau. Ein Auffrischen der Schwefelsäure (Wiederherstellen der
Ausgangskonzentration von 15-20%) ist aufgrund der geringen Schichtstärken nur selten nötig.
- An der Kathode (Minuspol) entsteht gasförmiger Wasserstoff, der bei größeren Mengen wegen der Explosionsgefahr (Wasserstoff
ist geruch-, geschmack- und farblos!) abgeführt werden muss.
2.3 Aufbau der Eloxalschicht
Zuerst entsteht elektrolytisch im Schwefelsäurebad eine geschlossene Schicht, die bei weiterem Wachstum in feine
kapillarähnliche Poren übergeht:
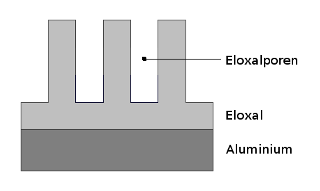
In diese Poren können sich nun Farbstoffmoleküle einlagern:
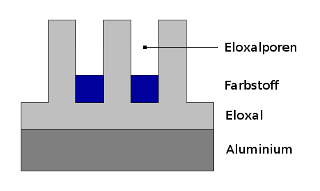
Zum Schluß werden die Poren durch Versiegeln (auch „Sealing“ genannt) verschlossen.
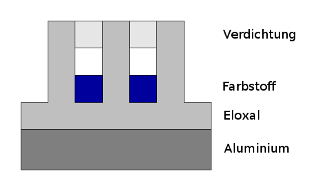
Die Farbe wird also nicht aufgetragen, sondern ist Bestandteil der Eloxalschicht und somit sehr gut gegen Abrieb
und chemische Einflüsse geschützt.



